Startup
イスラエルのDiA Imagingが、AIによる超音波解析の拡大に1400万ドルを獲得
深層学習と機械学習を利用して超音波スキャンの分析を自動化しているイスラエルのAIヘルステック企業DiA Imaging Analysisは、1400万ドルのシリーズBラウンドの資金調達を完了しました。DiAが前回資金調達を行ってから3年後の今回の成長ラウンドでは、新規投資家のAlchimia Ventures、Downing Ventures、ICON Fund、Philips、XTX Venturesに加え、CE Ventures、Connecticut Innovations、Defta Partners、Mindset Ventures、Dr Shmuel Cabillyなどの既存投資家も参加しています。DiAは、これまでに総額2,500万ドルを調達しています。
DiAは、今回の資金調達により、引き続き製品群を拡大し、超音波診断ベンダー、PACS/医療IT企業、再販業者、販売業者との新規および拡大したパートナーシップを目指すとともに、3つの地域市場でのプレゼンスを構築していきます。
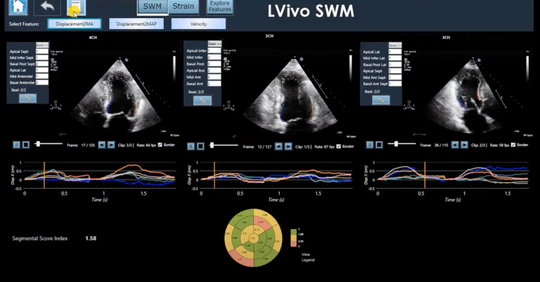
DiAは、臨床医や医療従事者向けに、超音波画像の撮影・解析を支援するAI支援ソフトウェアを販売しています。超音波画像の撮影・解析は、手動で行う場合、スキャンデータを視覚的に解釈する人間の専門知識が必要となります。そこでDiAは、自社のAI技術を「現在行われている手動および視覚的な推定プロセスから主観性を取り除く」とアピールしています。
DiAは、超音波画像を評価して、重要な詳細情報を自動的に見つけたり、異常を特定したりするようにAIを訓練しています。超音波分析に関連するさまざまな臨床的要件を対象とした製品を提供しており、その中には心臓に焦点を当てた製品も含まれています。例えば、同社のソフトウェアを使用して、駆出率、右心室のサイズと機能などの側面を測定・分析したり、冠動脈疾患の検出支援を行ったりすることができます。また、超音波のデータを利用して、膀胱の容積を自動で測定する製品もあります。
DiAのAIソフトウェアは、人間の目が境界線を検出したり、動きを識別したりする方法を模倣しており、人間の「主観的な」分析よりも進歩しており、スピードと効率の向上をもたらしていると主張しています。
CEO兼共同設立者のHila Goldman-Aslan氏は、次のように述べています。「当社のソフトウェアツールは、正しい画像の取得と超音波データの解釈の両方を必要とする臨床医をサポートするツールです。DiAのAIベースの解析機能は、北米や欧州を含む約20の市場で使用されています。中国では、パートナーが自社の機器の一部としてソフトウェアを使用する承認を得ています。同社は、超音波診断システムやPACSシステムのアドオンとしてソフトウェアを提供するチャネルパートナー(GE、フィリップス、コニカミノルタなど)と協力して市場開拓戦略を展開しています。当社の技術はベンダーニュートラルで、クロスプラットフォームなので、どんな超音波装置や医療ITシステムでも動作します。だからこそ、機器メーカーやヘルスケアIT/PACS企業と10社以上のパートナーシップを結んでいるのです。私が知っている限り、この分野のスタートアップで、このような能力、商業的な牽引力、多くのFDA/CE AIベースのソリューションを持つ企業は他にありません。現在までに、心臓と腹部の分野で7つのFDA/CE承認されたソリューションがあり、さらに多くのソリューションが控えています。AIの性能は、もちろん、学習されたデータセットに依存します。トレーニングデータに偏りがあると、トレーニングデータにあまり含まれていない患者グループの病気のリスクを誤診したり、過小評価したりする欠陥モデルになる可能性があるからです。超音波画像の重要なディテールを見分けることができるようにAIをどのように訓練したかについて、私たちは、多くの医療施設から何十万枚もの超音波画像にアクセスできるため、自動化されたエリアから別のエリアへと素早く移動することができます。私たちは、さまざまな病理学的特徴を持つ多様な人々のデータや、さまざまな機器からのデータを収集しています。"Garbage in Garbage out "という言葉があります。重要なのは、ゴミを持ち込まないことです。私たちのデータセットは、長年の経験を持つ専門家である複数の医師や技術者によってタグ付けされ、分類されています。また、誤って撮影された画像を拒否する強力な拒否システムも備えています。このようにして、データの取得方法の主観性を克服しています。」
なお、DiAが取得したFDAのクリアランスは510(k)クラスIIの承認であり、FDAに製品のPMA(Premarket Approval)を申請していない(するつもりもない)ことを確認しました。510(k)ルートは、多くの種類の医療機器を米国市場に投入する際の承認を得るために広く利用されています。しかし、510(k)ルートは、より厳格なPMAプロセスと同じレベルの精査を必要としない、軽いタッチのプロセスであると批判されています。
さらに言えば、急速に発展しているAI技術に対する規制は、その適用方法の発展に遅れがちであり、ヘルスケア分野への進出も含めて、大きな期待が寄せられている一方で、艶やかなマーケティングに応えられない場合には深刻なリスクがあるため、機器メーカーが約束した内容と、その機器が実際にどの程度規制の監視を受けているかの間には、いまだにギャップがあると言えます。例えば欧州連合(EU)では、機器の健康、安全、環境に関する基準を定めたCEスキームでは、メーカーは単に適合性を自己宣言するだけで、実際に主張する基準を満たしているかどうかを第三者が検証することはできません。しかし、AIのような新しい技術の安全性を規制するための厳格な制度とは考えられていません。そのため、EUでは現在、「高リスク」とされるAIの用途に特化した適合性評価を、次期人工知能法に基づいて追加導入しようとしています。
DiAのAIによる超音波診断のようなヘルスケア分野での利用は、ほぼ確実にこの分類に該当するため、AIAの下で何らかの追加規制要件が課せられることになるでしょう。しかし今のところ、表に出ている提案はEUの共同立法者によって討議されており、リスクのあるAIの利用に対する専用の規制制度が、この地域で発効するのはまだ何年も先のことです。
関連ニュース







最新ニュース

AIコード検証のSonar、AIネイティブ・コードレビューのGitarを買収しエージェント時代の統合プラットフォームへ
2026/05/22

フルスタックロボティクスのGenesis AI、X/Tesla出身のシニアエグゼクティブを迎え法務と運用の経営陣を拡充
2026/05/22

AIデータセキュリティのCyera、設立わずか5カ月のスタートアップGenie Securityを約5,000万ドルで買収
2026/05/22

AI駆動の心血管イメージングのCleerly、ロサンゼルス郡で初めて全システム導入
2026/05/22

サイバーセキュリティのBugcrowd、AIモデルが実環境のセキュリティスキルを習得するための強化学習環境RL Environmentsをリリース
2026/05/22